- Aula de Formación: Manejo terapéutico de la leishmaniosis desde el paciente seropositivo sano hasta aquel con enfermedad renal avanzada
patrocinado por:


Contenidos
Haz clic en los distintos apartados para ir al contenido
WhatsVet
Módulo: Tengo un seropositivo sano, ¿qué hago? patrocinado por Leisguard® de Ecuphar
Autoría: Anna Vila, LV, Dipl ECVIM, Servicio de Medicina Interna en Hospital Veterinario Universidad Católica de Valencia (UCV) y Xavier Roura, LV, PhD, Dipl ECVIM-CA, Hospital Clínic Veterinari Universitat Autònoma de Barcelona (UAB)
Podcasts
10 audiotips: ¿Siempre que tengo un positivo en serología tengo que tratar? patrocinado por Leisguard® de Ecuphar
Autoría: Anna Vila, LV, Dipl ECVIM, Servicio de Medicina Interna en Hospital Veterinario Universidad Católica de Valencia (UCV) y Xavier Roura, LV, PhD, Dipl ECVIM-CA, Hospital Clínic Veterinari Universitat Autònoma de Barcelona (UAB)
WhatsVet
Módulo: Cuando la leishmaniosis afecta a la funcionalidad renal patrocinado por Leisguard® de Ecuphar
Autoría: Anna Vila, LV, Dipl ECVIM, Servicio de Medicina Interna en Hospital Veterinario Universidad Católica de Valencia (UCV) y Xavier Roura, LV, PhD, Dipl ECVIM-CA, Hospital Clínic Veterinari Universitat Autònoma de Barcelona (UAB)
Podcasts
10 audiotips: ¿Qué hacemos con un paciente con leishmaniosis en el que diagnosticamos enfermedad renal? patrocinado por Leisguard® de Ecuphar
Autoría: Anna Vila, LV, Dipl ECVIM, Servicio de Medicina Interna en Hospital Veterinario Universidad Católica de Valencia (UCV) y Xavier Roura, LV, PhD, Dipl ECVIM-CA, Hospital Clínic Veterinari Universitat Autònoma de Barcelona (UAB)
Leisguard® de Ecuphar
Manejo terapéutico de la leishmaniosis desde el paciente seropositivo sano hasta aquel con enfermedad renal avanzada
Folleto Leisguard® - 10 años de experiencia
Conoce los resultados de más de una década de uso de Leisguard® en la prevención de la leishmaniosis canina. Datos clínicos reales, eficacia comprobada y su papel en programas preventivos en el arco mediterráneo.
Minidíptico Leispro® para Propietarios
Guía práctica para tutores de perros sobre cómo prevenir la leishmaniosis con el programa Leispro®. Información clara, sencilla y con garantía, ideal para acompañar la consulta veterinaria.
Post para Veterinarios – Programa Leispro®
Material visual para consulta o redes sociales. Explica de forma sintética los 3 pasos del programa preventivo Leispro® para proteger frente a la leishmaniosis: test, repelente y Leisguard®.
Folleto Leisguard®
Folleto informativo con los beneficios clave de Leisguard® como inmunomodulador. Ideal para explicar a clientes o en campañas de concienciación la importancia de su uso en zonas endémicas.
Anuncio Leisguard® para Seropositivos
Campaña gráfica enfocada en perros seropositivos sanos. Promueve el uso de Leisguard® como estrategia para evitar el desarrollo de la enfermedad clínica. Si quieres más información, consulta con tu delegado comercial de zona.
Cavalera et al. (2021) – Efecto de Leisguard® en Leishmaniosis y ERC
Estudio clínico que evalúa el impacto de domperidona en perros con leishmaniosis y enfermedad renal crónica. Resultados prometedores en marcadores inflamatorios y función renal.
Cavalera et al. (2022) – Domperidona + dieta renal
Ensayo clínico que demuestra cómo el uso combinado de Leisguard® y dieta renal puede ralentizar la progresión de la enfermedad renal crónica en perros con leishmaniosis.
Baxarias et al. (2023) – Leisguard® en perros seropositivos sanos
Ensayo clínico multicéntrico que avala la eficacia preventiva de Leisguard® en perros seropositivos asintomáticos. Menor progresión a enfermedad y excelente perfil de seguridad.
Formación WhatsApp
Microlearning vía WhatsApp
Módulo: Tengo un seropositivo sano, ¿qué hago?
Patrocinado por Leisguard® de Ecuphar

Anna Vila
LV, Dipl ECVIM, Servicio de Medicina Interna en Hospital Veterinario Universidad Católica de Valencia (UCV)

Xavier Roura
LV, PhD, Dipl ECVIM-CA, Hospital Clínic Veterinari Universitat Autònoma de Barcelona
Módulo: Tengo un seropositivo sano, ¿qué hago?
Parte 1


1.1
Haz clic en la imagen para obtener una vista más ampliada
¿Qué implica tener un perro seropositivo sano para leishmaniosis?
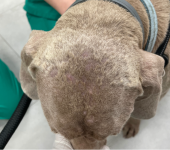
Una serología positiva frente a Leishmania spp. no siempre implica enfermedad activa. Muchos perros expuestos al parásito desarrollan una respuesta inmune eficaz que controla la infección sin mostrar síntomas. Un perro seropositivo sano es aquel que presenta anticuerpos frente a Leishmania spp. sin mostrar signos clínicos o clinicopatológicos relevantes. Esto implica que muchos perros pueden estar expuestos al parásito sin desarrollar enfermedad activa. Sin embargo, estos animales pueden ser portadores subclínicos y, bajo ciertas condiciones (estrés, inmunosupresión), la infección puede reactivarse. Identificar correctamente el estado inmunológico del animal permite tomar decisiones terapéuticas adecuadas y evitar tratamientos innecesarios.
Figura 1. Perra seropositiva a Leishmania.
1.2
Haz clic en la imagen para obtener una vista más ampliada
Prevalencia de la leishmaniosis en España
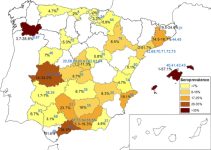
La leishmaniosis es endémica en la cuenca mediterránea, con una seroprevalencia variable en diferentes regiones de España. Estudios recientes indican que las Islas Baleares registran la cifra más alta (57,1 %) y Vizcaya sin casos detectados (0 %) 2. Esta variabilidad se debe a factores ambientales, climáticos y a la densidad del principal vector en España Phlebotomus perniciosus. En la mayoría de las zonas endémicas, más del 30 % de los perros son seropositivos. Sin embargo, no todos los perros infectados desarrollan signos clínicos, ya que muchos permanecen asintomáticos y actúan como reservorios. La detección temprana es clave para implementar medidas preventivas y reducir el riesgo de progresión de la enfermedad.4
Figura 2. Seroprevalencia de L. infantum canina en España por provincias, basado en una revisión de la literatura publicada entre 1985 y 2019.2
1.3
Haz clic en la imagen para obtener una vista más ampliada
Diagnóstico serológico: ventajas y limitaciones
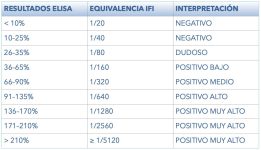
Las pruebas serológicas, como la inmunofluorescencia indirecta (IFI) y ELISA, son herramientas clave para detectar anticuerpos contra Leishmania, pero no diferencian entre infección activa y exposición pasada. Su sensibilidad y especificidad pueden variar según el método y el estadio de la enfermedad, lo que puede generar falsos negativos en infecciones tempranas.1 Títulos elevados de anticuerpos suelen indicar una infección en curso, pero no siempre se correlacionan con enfermedad clínica. Por ello, es fundamental complementar la serología con pruebas como la PCR, el proteinograma y la evaluación clínica. La combinación de estas técnicas permite una detección más precisa para así elegir el tratamiento y el seguimiento adecuado en perros seropositivos asintomáticos.5,6
Figura 3. Equivalencias en serología de los resultados obtenidos mediante los métodos IFI y ELISA para la detección de Leishmania.
1.4
Haz clic en la imagen para obtener una vista más ampliada
PCR: ¿Cuándo y por qué realizarla en perros seropositivos sanos?
La PCR confirma la infección por Leishmania al detectar ADN del parásito en distintos tejidos. Su sensibilidad supera el 90 % en médula ósea, bazo, ganglios y lesiones dermatológicas u oculares. Es útil en casos con serología dudosa o infecciones subclínicas que podrían progresar. Una PCR negativa no descarta la infección, pero reduce la probabilidad de enfermedad activa.
La PCR cuantitativa evalúa la carga parasitaria y monitoriza el tratamiento. Se recomienda en tejidos con menor presencia del parásito, como la sangre, donde una alta parasitemia indica enfermedad activa. Combinada con serología y otros parámetros, optimiza el diagnóstico y tratamiento.5,6,7
Figura 4. Esquematización del valor pronóstico de la PCR en casos dudosos deleishmaniosis canina. (Martínez et al., 2011)

Módulo: Tengo un seropositivo sano, ¿qué hago?
Parte 2


2.1
Haz clic en la imagen para obtener una vista más ampliada
Complejos inmunes circulantes (CIC): un posible nuevo biomarcador en la leishmaniosis canina
Los CIC juegan un papel clave en la leishmaniosis canina, contribuyendo al daño renal, vasculitis y otros procesos inflamatorios. Un estudio reciente validó un ELISA específico para medir CIC en perros con Leishmania infantum, mostrando una fuerte correlación entre niveles elevados y enfermedad avanzada.8 Los perros que responden bien al tratamiento reducen progresivamente los CIC, mientras que aquellos con recaídas los mantienen elevados. De hecho, un valor >1.539 se ha identificado como umbral óptimo para predecir recaídas. Estos hallazgos sugieren que la cuantificación de CIC podría ser útil para evaluar la progresión de la enfermedad, la respuesta al tratamiento y la detección temprana de recaídas.
Figura 5. Reconstrucción visual de anticuerpos en el torrente sanguíneo. Fuente: propia.
2.2
Haz clic en la imagen para obtener una vista más ampliada
Evaluación hematológica, bioquímica y de coagulación
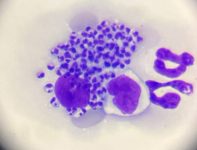
El hemograma y la bioquímica son esenciales para evaluar el estado sistémico del paciente. El hemograma suele revelar anemia no regenerativa (por inflamación crónica o enfermedad renal), trombocitopenia y posibles alteraciones leucocitarias (leucocitosis o leucopenia).4 Las alteraciones en la coagulación son comunes, con signos como la epistaxis. Algunas de estas son trombocitopatías, hipofibrinogenemia, aumentos en los tiempos de protrombina y tiempo parcial de tromboplastina activado, así como disminuciones de la antitrombina III.6 Además, la hipercoagulabilidad es un riesgo en pacientes con hipoalbuminemia, pese a que no podría predecirse a partir de los niveles de albúmina en pacientes con nefropatía perdedora de proteínas.
Figura 6. Amastigotes de Leishmania en sangre periférica. La visualización de amastigotes en sangre periférica ocurre en menos del 5 % de los pacientes con leishmaniosis. Fuente: propia.
2.3
Haz clic en la imagen para obtener una vista más ampliada
Evaluación de la función renal
La leishmaniosis puede causar daño renal progresivo, siendo la glomerulonefritis inmunomediada la lesión más frecuente por la deposición de inmunocomplejos.7 El urianálisis y la relación proteína/creatinina urinaria (UPC) son clave para detectar proteinuria, uno de los primeros signos de afectación renal, y para el estadiaje según las guías IRIS. La proteinuria persistente puede derivar en enfermedad renal crónica (ERC) si no se trata. Es esencial monitorizar urea, creatinina, fósforo sérico y presión arterial, ya que la hipertensión es frecuente en perros con leishmaniosis (29-62 % de los casos). Se recomienda control regular de la presión arterial en perros con nefropatía proteinúrica.7 La detección temprana y el manejo adecuado ayudan a prevenir el deterioro renal severo y mejorar el pronóstico.7
Figura 7. Paciente que se mantuvo persistentemente proteinúrico tras desarrollar glomerulonefritis por Leishmania. Fuente: propia.
2.4
Haz clic en la imagen para obtener una vista más ampliada
Manejo del perro seropositivo sano: ¿tratar o no tratar?
El manejo de perros seropositivos asintomáticos debe ser individualizado. Si el perro presenta títulos serológicos bajos, ausencia de carga parasitaria detectable por PCR y pruebas complementarias normales (proteinograma, proteína C reactiva, hematología, bioquímica y urianálisis), el tratamiento específico con antimoniales o miltefosina no está indicado y el tratamiento con alopurinol podría conllevar resistencias futuras. Sin embargo, se puede considerar la administración de inmunomoduladores como la domperidona (Leisguard®) para potenciar la respuesta inmune y prevenir la progresión clínica.7 En estos casos, la decisión clínica debe individualizarse, se aconseja un control periódico cada 3-6 meses, evaluando serología, PCR y alteraciones clínicopatológicas.4
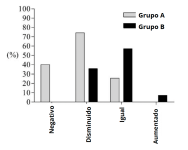
Figura 8. Resultados de un estudio en el que se demostró una disminución del título de anticuerpos en el 74,3 % de los pacientes, y una seroconversión (resultado serológico negativo) del 40 % de los mismos, tras la utilización de domperidona como tratamiento (Gómez-Ochoa et al., 2009).

Módulo: Tengo un seropositivo sano, ¿qué hago?
Parte 3


3.1
Haz clic en la imagen para obtener una vista más ampliada
Uso de domperidona en perros seropositivos
La domperidona, principio activo de Leisguard®, es un inmunomodulador que estimula la respuesta inmune celular tipo Th1, promoviendo la producción de interferón-γ. Esta respuesta es clave para controlar la Leishmania, ya que favorece la acción fagocítica de los macrófagos. En perros seropositivos, puede ayudar a mantener el equilibrio inmunológico y reducir la carga parasitaria, minimizando el riesgo de progresión. Su uso profiláctico se indica en pacientes con alto riesgo de exposición y en perros con títulos bajos o moderados, sin signos clínicos, especialmente si hay riesgo elevado de progresión. Estudios han demostrado que disminuye títulos serológicos y mejora biomarcadores inflamatorios. El tratamiento debe ir acompañado de seguimiento regular con serología y PCR.9
3.2
Haz clic en la imagen para obtener una vista más ampliada
Evaluación hematológica, bioquímica y de coagulación
Un perro seropositivo sano debe ser monitorizado periódicamente para detectar cualquier cambio que sugiera progresión de la infección. El seguimiento clínico debe incluir examen físico completo y evaluación de signos inespecíficos. Se recomienda realizar controles cada 3-6 meses, incluyendo proteinograma y serología cuantitativa. En casos dudosos, se pueden usar marcadores tempranos como proteína C reactiva o PCR cuantitativas en sangre para evaluar carga parasitaria y riesgo de recidiva. Además, deben hacerse hemograma, bioquímica sérica y urianálisis para identificar alteraciones hematológicas, hepáticas o renales, prestando especial atención a la proteinuria como marcador temprano de nefropatía.4 Un seguimiento adecuado permite intervenciones tempranas y mejora el pronóstico.
Figura 10. Protocolo de monitorización recomendado. Tabla basada en las guías Leishvet.
3.3
Haz clic en la imagen para obtener una vista más ampliada
Signos clínicos sutiles en perros seropositivos subclínicos: la importancia de la observación
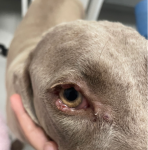
Un perro seropositivo puede permanecer asintomático durante meses o años antes de desarrollar enfermedad clínica.8 No obstante, ciertos signos sutiles pueden indicar progresión. Entre los más comunes: pérdida de peso, letargia, hepatoesplenomegalia, linfadenopatía leve, dermatitis seca o alopecia focal. También pueden observarse colitis o hematoquecia (30 %), signos oculares (uveítis, conjuntivitis), cojeras o lesiones articulares. A nivel clinicopatológico, la presencia de proteinuria, hipoalbuminemia, trombocitopenia o anemia leve no regenerativa puede ser un indicio temprano. Educar al tutor para que detecte cambios en comportamiento, apetito o apariencia es clave para identificar precozmente una evolución negativa.4,7
Figura 11. Paciente con signos dermatológicos de leishmania sutiles que a los pocos meses avanzan a signos más graves como la uveítis. Fuente: propia.
3.4
Haz clic en la imagen para obtener una vista más ampliada
Impacto de la coinfección en perros seropositivos sanos
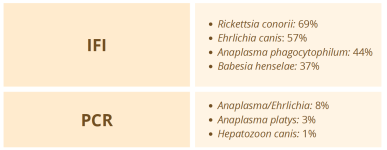
Los perros seropositivos sanos pueden verse afectados por coinfecciones con otros patógenos como Ehrlichia, Anaplasma, Dirofilaria o Babesia, que también son transmitidos por vectores. En algunos casos como la coinfección por ehrlichiosis puede ser hasta de un 30 % de los perros. Estas coinfecciones pueden alterar la respuesta inmune y favorecer la reactivación de la infección por Leishmania, complicando el diagnóstico y el tratamiento. Por otra parte, también es importante evaluarlos como un factor pronóstico negativo como en el caso de Anaplasma. Evaluar la posible presencia de coinfecciones mediante pruebas serológicas y moleculares es clave para establecer un manejo terapéutico adecuado. En caso de coinfección, se deben tratar ambas enfermedades y considerar la terapia inmunomoduladora para fortalecer la respuesta inmunitaria del perro y reducir el riesgo de progresión clínica. Un enfoque diagnóstico integral garantiza un control más efectivo de la salud del paciente.
Figura 12. Coinfecciones de pacientes con leishmaniosis detectadas en un estudio realizado en España (M. Baxarias et al., 2018).

Módulo: Tengo un seropositivo sano, ¿qué hago?
Parte 4


4.1
Haz clic en la imagen para obtener una vista más ampliada
Importancia de la presión arterial en perros seropositivos
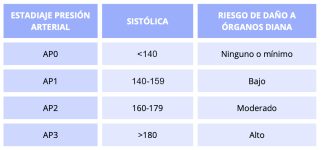
La hipertensión sistémica es una complicación frecuente en perros seropositivos con afectación renal, especialmente en aquellos con proteinuria persistente. Estudios indican que entre el 29 % y el 62 % de los perros con leishmaniosis desarrollan hipertensión. Esta se asocia con una mayor proteinuria, una disminución de la tasa de filtración glomerular y una progresión acelerada hacia enfermedad renal crónica.7 Se recomienda realizar mediciones regulares de la presión arterial, especialmente en perros con signos de nefropatía o proteinuria significativa, siguiendo los consejos de las Guías IRIS. El tratamiento temprano con inhibidores de la enzima convertidora de angiotensina (IECA) u otros antihipertensivos puede ralentizar el deterioro renal y mejorar el pronóstico a largo plazo.
Figura 13. Riesgo de daño a órganos diana por hipertensión. Basada en las Guías IRIS.
4.2
Haz clic en la imagen para obtener una vista más ampliada
Medidas de prevención
La prevención es clave en la leishmaniosis. El control vectorial reduce el riesgo de transmisión y reinfección mediante collares (deltametrina), pipetas tópicas o sprays repelentes (imidacloprid y permetrina).1 Evitar paseos durante las horas de mayor actividad del vector (amanecer y atardecer) también reduce el riesgo de picaduras.4 La vacunación es otra medida clave, aunque no se recomienda en perros seropositivos al no estar suficientemente evaluada.
Los inmunomoduladores refuerzan la respuesta inmune Th1, promoviendo resistencia frente a la infección. El uso profiláctico de domperidona (Leisguard®) en perros seronegativos expuestos reduce la seroconversión, y en seropositivos asintomáticos con títulos bajos contribuye a mantener la infección subclínica. También mejora biomarcadores inmunológicos.9
Figura 14. La protección de nuestros pacientes mediante los distintos métodos disponibles es crucial. Fuente: propia.
4.3
Haz clic en la imagen para obtener una vista más ampliada
¿Puede un perro seropositivo volver a ser seronegativo?
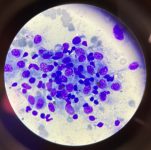
Algunos perros seropositivos pueden experimentar una disminución en sus títulos de anticuerpos con el tiempo, especialmente si tienen una respuesta inmunitaria efectiva o han recibido tratamiento.4 Sin embargo, la seroconversión completa es rara y no significa que el parásito haya sido eliminado del organismo. Leishmania infantum puede persistir en tejidos como la médula ósea o los ganglios linfáticos en niveles indetectables.6 Si un perro previamente seropositivo da negativo en serología, no siempre significa que haya eliminado la infección. En estos casos, si existen dudas o signos clínicos, puede ser útil realizar pruebas adicionales, repitiendo el proteinograma o realizando una PCR para obtener un cuadro más preciso.4
Figura 15. Paciente con hepatitis por Leishmania. Se observan en la imagen los amastigotes de Leishmania en una citología hepática. Fuente: propia.
4.4
Haz clic en la imagen para obtener una vista más ampliada
Una serología negativa NO descarta la enfermedad
Un resultado serológico negativo no siempre descarta la infección por Leishmania infantum. En fases iniciales, los perros pueden tardar meses en desarrollar anticuerpos detectables (entre 1 y 22 meses), especialmente si la carga parasitaria es baja.6 Además, la serología puede dar falsos negativos en perros inmunosuprimidos o en estadios muy tempranos de la infección, ya que la respuesta humoral puede ser insuficiente para ser detectada. De hecho, la sensibilidad de la serología varía entre un 30 y un 70 %, dependiendo del método utilizado y del estado inmunológico del paciente.6 En perros con sospecha clínica y serología negativa, se recomienda repetir la prueba semanas después, ya que la seroconversión puede retrasarse mucho. Si persisten dudas, la detección del ADN del parásito mediante PCR puede ayudar a confirmar la infección.6
Figura 16. Amastigotes de Leishmania. Fuente: propia.

Módulo: Tengo un seropositivo sano, ¿qué hago?
Parte 5


5.1
Haz clic en la imagen para obtener una vista más ampliada
¿Puede transmitirse la Leishmania sin la picadura de un flebótomo?
La principal vía de transmisión de Leishmania es la picadura de flebótomos infectados, pero existen otras formas menos frecuentes. Se ha demostrado la transmisión vertical de madre a cachorro,11 y la transmisión venérea. Existe un riesgo alto por transfusiones sanguíneas si el donante está infectado.12
Aunque se ha detectado ADN de Leishmania en garrapatas, no se ha confirmado su papel como vectores competentes.13 Así como tampoco hay evidencia suficiente en cuanto a la transmisión por contacto directo (mordeduras o heridas).14
Para prevenir la transmisión vertical, se recomienda evitar la reproducción en perras seropositivas y retirar de los programas de reproducción a machos positivos.4 En transfusiones, la serología y PCR en donantes son esenciales para prevenir la transmisión iatrogénica.7
Figura 17. Ilustración de las distintas formas planteadas de transmisión de Leishmania que no son la transmitida por flebotomos. Fuente: propia.
5.2
Haz clic en la imagen para obtener una vista más ampliada
El proteinograma: más allá del diagnóstico
El proteinograma es una herramienta clave para evaluar la respuesta inmune y la fase de la infección en perros seropositivos. La hipergammaglobulinemia, junto con la disminución de la relación albúmina/globulina son indicativos de una respuesta inmunitaria activa y por lo tanto, una posible progresión de la enfermedad. El ratio albúmina/globulina puede ser un marcador temprano de infección activa, ya que se altera antes de los signos clínicos.8 Estos parámetros pueden orientar sobre la necesidad de un seguimiento más estricto y una posible intervención terapéutica precoz. Ante un resultado serológico positivo, valorar el proteinograma junto a otros parámetros sanguíneos y urinarios, proporciona una visión integral del estado del paciente y permite ajustar el manejo clínico de manera más precisa.
Figura 18. Alteraciones típicas que observamos en el proteinograma de pacientes con Leishmania.
5.3
Haz clic en la imagen para obtener una vista más ampliada
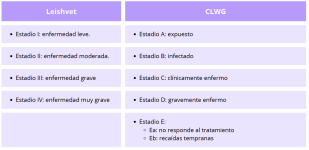
Estadificación clínica de la Leishmania: Leishvet vs. CLWG (Canine Leishmania Working Group)
La estadificación clínica de la leishmaniosis es clave para establecer pronóstico y guiar el tratamiento. Dos sistemas ampliamente utilizados son los de LeishVet y el Canine Leishmaniasis Working Group (CLWG). Ambos permiten evaluar la enfermedad, aunque con enfoques distintos. LeishVet clasifica en cuatro estadios (I-IV) según signos clínicos, serología, PCR, proteinograma y función renal. Este sistema se basa en la progresión clínica con criterios laboratoriales definidos, útil en la práctica diaria. El CLWG, en cambio, clasifica en cinco grupos, diferenciando entre exposición, infección activa y enfermedad manifiesta, e incluye categorías para recaídas y no respondedores. Ambos sistemas facilitan decisiones terapéuticas, seguimiento y evaluación pronóstica individualizada.
Figura 19. Comparación entre las dos distintas clasificaciones de leishmaniosis, Leishvet y Canine Leishmania Working Group Los estadios de ambas no son intercambiables.
5.4
Haz clic en la imagen para obtener una vista más ampliada
Manifestaciones menos comunes de la leishmaniosis
Aunque la leishmaniosis canina suele manifestarse con signos dermatológicos, linfadenopatía y enfermedad renal, existen formas atípicas menos frecuentes. La miositis ha sido descrita en algunos perros, por ejemplo, la masticatoria, con inflamación severa de los músculos temporales y maseteros.25,26 También, se han documentado casos de artritis tanto erosiva como no erosiva, con inflamación articular severa secundaria a la infección.27
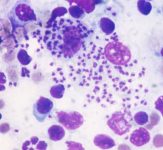
A nivel digestivo, la diarrea crónica de intestino delgado ha sido reportada en perros con leishmaniosis, encontrándose amastigotes en biopsias digestivas.24, 35 Se ha asociado también a casos de meningoencefalitis canina.28 Estas manifestaciones atípicas destacan la capacidad de Leishmania para afectar múltiples órganos y sistemas, lo que puede dificultar su diagnóstico.
Figura 20. Paciente con duodenitis por Leishmania. Esta paciente mostraba una serología negativa. Fuente: propia.
Bibliografía
- Sykes, J.E. et al. (2023) Greene’s Infectious Diseases of the dog and cat. St. Louis, MO: Elsevier.
- Gálvez, R. et al. (2020) ‘Latest trends in Leishmania infantum infection in dogs in Spain, part I: Mapped Seroprevalence and sand fly distributions’, Parasites & Vectors, 13(1). doi:10.1186/s13071-020-04081-7.
- Moreno, J. and Alvar, J. (2002) ‘Canine leishmaniasis: Epidemiological risk and the experimental model’, Trends in Parasitology, 18(9), pp. 399– doi:10.1016/s1471-4922(02)02347-4.
- Solano-Gallego, L. et al. (2011) ‘LEISHVET guidelines for the practical management of canine leishmaniosis’, Parasites & Vectors, 4(1). doi:10.1186/1756-3305-4-86.
- Roura, X. et al. (2013) ‘Prognosis and monitoring of leishmaniasis in dogs: A Working Group report’, The Veterinary Journal, 198(1), pp. 43– doi:10.1016/j.tvjl.2013.04.001.
- Paltrinieri, S. et al. (2010) ‘Guidelines for diagnosis and clinical classification of leishmaniasis in dogs’, Journal of the American Veterinary Medical Association, 236(11), pp. 1184– doi:10.2460/javma.236.11.1184.
- Roura, X. et al. (2020) ‘Canine leishmaniosis and kidney disease: Q&A for an overall management in clinical practice’, Journal of Small Animal Practice, 62(1). doi:10.1111/jsap.13237.
- Sarquis, J. et al. (2024) ‘Clinical validation of circulating immune complexes for use as a diagnostic marker of canine leishmaniosis’, Frontiers in Veterinary Science, 11. doi:10.3389/fvets.2024.1368929.
- Miró, G. et al. (2024) ‘New immunomodulatory treatment protocol for canine LEISHMANIOSIS reduces parasitemia and proteinuria’, PLOS Neglected Tropical Diseases, 18(12). doi:10.1371/journal.pntd.0012712.
- Iris guidelines (2023) IRIS. Available at: https://www.iris-kidney.com/iris-guidelines-1
- Ben Slimane, T. et al. (2014) ‘An investigation on vertical transmission of Leishmania infantum in experimentally infected dogs and assessment of offspring’s infectiousness potential by xenodiagnosis’, Veterinary Parasitology, 206(3–4), pp. 282– doi:10.1016/j.vetpar.2014.10.020.
- Silva, F.L. et al. (2009) ‘Venereal transmission of canine visceral leishmaniasis’, Veterinary Parasitology, 160(1–2), pp. 55– doi:10.1016/j.vetpar.2008.10.079.
- Dantas-Torres, F. (2011) ‘Ticks as vectors of Leishmania parasites’, Trends in Parasitology, 27(4), pp. 155– doi:10.1016/j.pt.2010.12.006.
- Naucke, T.J., Amelung, S. and Lorentz, S. (2016) ‘First report of transmission of canine leishmaniosis through bite wounds from a naturally infected dog in Germany’, Parasites & Vectors, 9(1). doi:10.1186/s13071-016-1551-0.
- Nabity, M.B. (2018) ‘Traditional renal biomarkers and new approaches to diagnostics’,
- Toxicologic Pathology, 46(8), pp. 999–1001. doi:10.1177/0192623318800709.
- Ruiz, P. et al. (2024) Urinary neutrophil gelatinase-associated lipocalin as early biomarker for renal disease in dogs with leishmaniosis [Preprint]. doi:10.2139/ssrn.4757995.
- Ruiz, P. et al. (2023) ‘Urinary cystatin C and N-acetyl-beta-D-glucosaminidase (NAG) as early biomarkers for renal disease in dogs with leishmaniosis’, Veterinary Parasitology, 318, p. 109930. doi:10.1016/j.vetpar.2023.109930.
- Pantaleo, V. et al. (2024) ‘Short term treatment monitoring of renal and inflammatory biomarkers with naturally occurring leishmaniosis: A cohort study of 30 dogs’, Veterinary Sciences, 11(11), p. 517. doi:10.3390/vetsci11110517.
- Aresu, L. et al. (2012) ‘Light and electron microscopic analysis of consecutive renal biopsy specimens from leishmania-seropositive dogs’, Veterinary Pathology, 50(5), pp. 753– doi:10.1177/0300985812459336.
- Cortadellas, O. et al. (2006) ‘Systemic hypertension in dogs with leishmaniasis: Prevalence and clinical consequences’, Journal of Veterinary Internal Medicine, 20(4), p. 941. doi:10.1892/0891-6640(2006)20[941:shidwl]2.0.co;2.
- Costa, F.A. et al. (2003) ‘Histopathologic patterns of nephropathy in naturally acquired canine visceral leishmaniasis’, Veterinary Pathology, 40(6), pp. 677– doi:10.1354/vp.40-6-677.
- Peris, M.P. et al. (2020) ‘Neutrophil gelatinase-associated lipocalin (NGAL) is related with the proteinuria degree and the microscopic kidney findings in Leishmania-infected dogs’, Microorganisms, 8(12), p. 1966. doi:10.3390/microorganisms8121966.
- López, M.C. et al. (2022) ‘Chronic diarrhea secondary to canine leishmaniosis: Case series’, Comparative Immunology, Microbiology and Infectious Diseases, 90–91, p. 101897. doi:10.1016/j.cimid.2022.101897.
- Santos, B.G. et al. (2021) ‘Focal myositis associated with Leishmania spp. infection in a dog – diagnostic approach’, Ciência Rural, 51(2). doi:10.1590/0103-8478cr20200247.
- Vamvakidis, C.D. et al. (2000) ‘Masticatory and skeletal muscle myositis in canine leishmaniasis (leishmania infantum)’, Veterinary Record, 146(24), pp. 698– doi:10.1136/vr.146.24.698.
- Sbrana, S. et al. (2014) ‘Retrospective study of 14 cases of canine arthritis secondary to leishmania infection’, Journal of Small Animal Practice, 55(6), pp. 309– doi:10.1111/jsap.12204.
- Zdora, I. et al. (2022) ‘Case report: Lympho-histiocytic meningoencephalitis with central nervous system vasculitis of unknown origin in three dogs’, Frontiers in Veterinary Science, 9. doi:10.3389/fvets.2022.944867.
- Camoletto, D.A. et al. (2020) ‘Alteraciones Ecográficas y hematológicas en caninos con leishmaniosis visceral’, Revista Veterinaria, 31(1), pp. 57–60. doi:10.30972/vet.3114632.
- Lucero, M. et al. (2019) `A plasma calcium-phosphorus product can be used to predict the lifespan of dogs with chronic kidney disease´, Can Vet Journal, PMC6855231
- Sarquis, J., et al. (2024). `Relapses in canine leishmaniosis: risk factors identified through mixed-effects logistic regression.´ Parasites & Vectors, 17(1), 64. https://doi.org/10.1186/s13071-024-06423-1
- Digiaro, S., et al. (2024) ‘Treatment of canine leishmaniasis with meglumine antimoniate: a clinical study of tolerability and efficacy’, Animals, 14(15), p. 2244. doi: 10.3390/ani14152244
- Nogueira, F.S. et al. (2019) ‘Use of miltefosine to treat canine visceral leishmaniasis caused by Leishmania infantum in Brazil’, Parasites & Vectors, 12(1), p. 79. doi: 10.1186/s13071-019-3323-0. ResearchGate+2https://oalib.com+2PubMed+2
- García, M. et al. (2024) ‘Critically Appraised Topic on Canine Leishmaniosis: Does Treatment with Antimonials and Allopurinol Have the Same Clinical and Clinicopathological Efficacy as Treatment with Miltefosine and Allopurinol, after One Month of Treatment?’, Veterinary Sciences, 11(6), p. 231. doi: 10.3390/vetsci11060231.
- Vila A, Movilla R, Lloret A, Majó N, Marco AJ, et al. (2016) Chronic Small Bowel Diarrhea Due to Granulomatous Duodenitis by Leishmania in two Dogs. J Vet Med Res 3(1): 1040
- Cavalera MA, Gernone F, Uva A, Donghia R, Zizzadoro C, Zatelli A. Efficacy of domperidone plus renal diet in slowing the progression of chronic kidney disease in dogs with leishmaniosis. Parasit Vectors. 2022 Oct 31;15(1):397. doi: 10.1186/s13071-022-05537-8. PMID: 36316751; PMCID: PMC9620618.
- Jesus L, Arenas C, Domínguez-Ruiz M, Silvestrini P, Englar RE, Roura X, Leal RO. Xanthinuria secondary to allopurinol treatment in dogs with leishmaniosis: Current perspectives of the Iberian veterinary community. Comp Immunol Microbiol Infect Dis. 2022 Apr;83:101783. doi: 10.1016/j.cimid.2022.101783. Epub 2022 Feb 24. PMID: 35240487.
- Torres M, Pastor J, Roura X, Tabar MD, Espada Y, Font A, Balasch J, Planellas M. Adverse urinary effects of allopurinol in dogs with leishmaniasis. J Small Anim Pract. 2016 Jun;57(6):299-304. doi: 10.1111/jsap.12484. Epub 2016 Apr 26. PMID: 27112522.
Sigue formándote con "Aprende a prevenir y tratar la enfermedad periodontal y conoce todas sus posibles afectaciones sistémicas" de la mano de Dental.pet by Ecuphar


WhatsVet | La salud bucodental como parte fundamental de un plan de medicina preventiva en la clínica diaria
Autoría: Ignacio Velázquez, Ldo. Vet. Dipl. AVDC. Dipl. EVDC, Board Certified Veterinary DentistTM, EBVS® European Veterinary, Specialist in Dentistry.
Podcast | 10 Audiotips: Tips con los que mejorar la inclusión de la salud bucodental en nuestro plan de medicina preventiva
Autoría: Ignacio Velázquez, Ldo. Vet. Dipl. AVDC. Dipl. EVDC, Board Certified Veterinary DentistTM, EBVS® European Veterinary, Specialist in Dentistry.
WhatsVet | Módulo: Opciones profilácticas y terapéuticas para el mantenimiento de una adecuada salud bucodental
Autoría: Ignacio Velázquez, Ldo. Vet. Dipl. AVDC. Dipl. EVDC, Board Certified Veterinary DentistTM, EBVS® European Veterinary, Specialist in Dentistry.
Podcast | 11 Audiotips: Tips para el manejo de la enfermedad periodontal ya instaurada… cuando la medicina preventiva no ha sido suficiente
Autoría: Ignacio Velázquez, Ldo. Vet. Dipl. AVDC. Dipl. EVDC, Board Certified Veterinary DentistTM, EBVS® European Veterinary, Specialist in Dentistry.