- Aula de Formación: Expertos en Leishmaniosis, desde la prevención hasta el manejo global
patrocinado por:



Advantix®, Seresto®, Elanco y la barra diagonal son marcas registradas de Elanco o sus filiales. ©2024 Elanco Animal Health, Inc.o sus afiliadas. * Datos VetEvidence SellOutTAM Abr 24.
Contenidos
Haz clic en los distintos apartados para ir al contenido
WhatsVet
Módulo: Leishmaniosis canina y felina – ¿entendemos cómo funciona la enfermedad? patrocinado por Seresto® y Advantix® de Elanco
Autoría: María Dolores Tabar Rodríguez, DVM, Dip. EBVS® European Veterinary Specialist in Small Animal Internal Medicine, AniCura San Vicente Hospital Veterinario (San Vicente del Raspeig, Alicante).
Podcasts
10 audiotips: Cuando hablamos de leishmaniosis, ¿cómo puedo concienciar a mis clientes de que deben hacer una buena prevención? patrocinado por Seresto® y Advantix® de Elanco
Autoría: María Dolores Tabar Rodríguez, DVM, Dip. EBVS® European Veterinary Specialist in Small Animal Internal Medicine, AniCura San Vicente Hospital Veterinario (San Vicente del Raspeig, Alicante).
WhatsVet
Módulo: La prevención y la detección temprana como pilar fundamental del éxito clínico patrocinado por Seresto® y Advantix® de Elanco
Autoría: María Dolores Tabar Rodríguez, DVM, Dip. EBVS® European Veterinary Specialist in Small Animal Internal Medicine, AniCura San Vicente Hospital Veterinario (San Vicente del Raspeig, Alicante).
Podcasts
10 audiotips: Qué herramientas tengo para intentar evitar que un perro desarrolle una leishmaniosis clínica patrocinado por Seresto® y Advantix® de Elanco
Autoría: María Dolores Tabar Rodríguez, DVM, Dip. EBVS® European Veterinary Specialist in Small Animal Internal Medicine, AniCura San Vicente Hospital Veterinario (San Vicente del Raspeig, Alicante).
Seresto® y Advantix®
 Expertos en Leishmaniosis
Expertos en Leishmaniosis
MiElanco - Creces tú, crecemos todos
En MiElanco encontrarás servicios conocimientos y recursos de Elanco para ayudarte en tu práctica diaria con tus clientes. ¡Estás a un click de acceder a todos lo contenidos! Aquí tienes el codigo para tu registro: MiElancoDigitalPetShop2023
VETNIA es la comunidad de los profesionales de la salud animal
Un programa creado para reivindicar la importancia de la profesión veterinaria para la sociedad, apostar por el conocimiento, la formación y la salud de los profesionales, e impulsar el negocio de la clínica veterinaria
Portal Veterinario de Elanco
El espacio creado por y para los profesionales que amamos los animales y cuidamos su salud y bienestar, donde encontrarás materiales, formaciones y soluciones que te ayudarán en tu práctica diaria.
Fichas técnicas de Seresto® y Advantix®
Prevención más allá de los ectoparásitos
Seresto®: mecanismo de acción. Seresto® es un collar antiparasitario para perros y gatos. Combina dos principios activos: imidacloprid (10%) y flumetrina (4,5%).
Estudios sobre las CVBD
La leishmaniosis es una de las enfermedades caninas de transmisión vectorial (CVBD) más importante y de mayor gravedad, ya que puede ser mortal en perros.
Contenidos para tus redes sociales
Con el objetivo de poner luz sobre este riesgo, en Elanco iniciamos una campaña para concienciar a los propietarios sobre la importancia de proteger a su perro todos los días y noches del año.
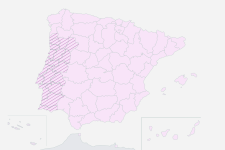
Mapa Elanco de prevalencia de enfermedades parasitarias
Debido al cambio climático, los parásitos y las enfermedades que transmiten, se pueden expandir a zonas donde no se encontraban anteriormente.
Formación WhatsApp
Microlearning vía WhatsApp
Módulo: Leishmaniosis canina y felina – ¿entendemos cómo funciona la enfermedad?
Patrocinado por Seresto® y Advantix® de Elanco

María Dolores Tabar Rodríguez
DVM, Dip. EBVS® European Veterinary Specialist in Small Animal Internal Medicine, AniCura San Vicente Hospital Veterinario (San Vicente del Raspeig, Alicante).
Módulo: Leishmaniosis canina y felina – ¿entendemos cómo funciona la enfermedad?
Parte 1


1.1
Haz clic en la imagen para obtener una vista más ampliada
Transmisión principal de la leishmaniosis
La leishmaniosis es una enfermedad infecciosa transmitida por la picadura de flebótomos hembra infectados. Estos insectos habitan en regiones cálidas como Europa, Asia, África, Australia y América. Existen más de mil especies, siendo Phlebotomus el género más relevante en el “viejo mundo” y Lutzomyia en el “nuevo mundo”. Las especies de Leishmania son muy específicas de su vector. En Europa, Leishmania infantum es la principal causante de leishmaniosis canina. En menor medida se han detectado L. tropica y L. major. En la cuenca mediterránea, los vectores más importantes son Phlebotomus perniciosus y Phlebotomus ariasi
1.2
Haz clic en la imagen para obtener una vista más ampliada
Características de los flebótomos
Los flebótomos llevan un estilo de vida terrestre, con ciclos de unas 6 semanas según temperatura, humedad y lluvias. Vuelan distancias cortas, de unos 300 metros, y son más activos al atardecer y por la noche, con temperaturas de 18-22ºC. Durante el día se refugian en lugares sombríos y húmedos como grietas, sótanos, madrigueras o establos.
El cambio climático y la acción humana han favorecido su expansión hacia zonas más del norte y con mayor altitud. Además, el calentamiento global puede alterar su estacionalidad, densidad y supervivencia, así como los períodos de incubación de los patógenos que transmiten.
1.3
Haz clic en la imagen para obtener una vista más ampliada
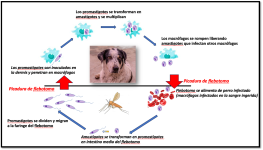
Ciclo de desarrollo del parásito
Leishmania spp. presenta dos formas: promastigote (flagelada, en el intestino del flebótomo) y amastigote (intracelular, en el hospedador). Su desarrollo en el vector dura 7-14 días si la temperatura supera los 18ºC. Luego, los promastigotes migran a la faringe.
La transmisión ocurre cuando la hembra se alimenta de sangre. En la piel, los promastigotes son fagocitados por macrófagos y células dendríticas, se transforman en amastigotes y se multiplican. Se diseminan por vía linfo-hemática a bazo, médula ósea y otros órganos. La incubación es variable, de 3 meses a años, según carga parasitaria, virulencia y respuesta inmune del hospedador.
Figura 3. Ciclo de desarrollo del parásito.
1.4
Haz clic en la imagen para obtener una vista más ampliada
Otras formas de transmisión de la leishmaniosis
Otras vías de transmisión son posibles y están demostradas, pero hay que recordar que la principal vía de transmisión es a través de la picadura de la hembra de flebótomo.
Es posible la transmisión a través de transfusiones sanguíneas, de ahí la importancia de testar a los donantes de sangre. También hay casos reportados de transmisión venérea, así como vertical; de hecho, en zonas no endémicas como Estados Unidos se cree que quizá la vía vertical transplacentaria sea una de las fundamentales fuentes de transmisión. Se han dado casos de transmisión por mordeduras en Estados Unidos y Alemania. En cuanto a si otros vectores son capaces de transmitir la leishmaniosis, de momento no hay evidencias: se ha detectado la presencia del parásito en garrapatas, pero por ahora no se ha demostrado que sean capaces de transmitirla.
Figura 4. La leishmaniosis se puede transmitir a través de transfusiones sanguíneas.

Módulo: Leishmaniosis canina y felina – ¿entendemos cómo funciona la enfermedad?
Parte 2


2.1
Haz clic en la imagen para obtener una vista más ampliada
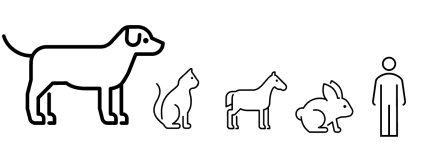
Especies a las que afecta la leishmaniosis
El perro se considera el principal hospedador de L. infantum. Otras especies de mamíferos pueden infectarse, incluido el gato y el hombre, y se ha aislado este parásito de roedores como ratas o ardillas, de lagomorfos (liebres), de caballos, gatos y canidos salvajes como el zorro rojo, lobos y chacales, aunque todavía no se ha establecido el papel de estos hospedadores en la infección.
Aunque los perros suponen el principal reservorio de la leishmaniosis, varios estudios han mostrado también evidencia de ciclos silvestres de transmisión en los que participan los vectores habituales, pero siendo los reservorios mamíferos salvajes, como conejos y liebres (de hecho, hubo un brote de leishmaniosis humana en la zona de Fuenlabrada hace unos años cuyo origen fueron las liebres).
Figura 5.
2.2
Haz clic en la imagen para obtener una vista más ampliada
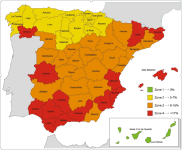
Distribución en España
En España había zonas en el Norte de España donde la infección hace años era muy rara, pero actualmente la distribución ha ido cambiando y aunque las prevalencias sean menores en algunas zonas, ahora se pueden diagnosticar casos de leishmaniosis en cualquier zona de la península. Además, tiene una distribución focal, haciendo que la endemicidad varíe mucho entre zonas geográficas, e incluso entre zonas cercanas (con nichos endémicos por mayor abundancia del vector y mayor prevalencia en animales reservorios).
En el siguiente mapa se pueden reflejar las seroprevalencias en diferentes zonas de España, según el trabajo realizado por Gálvez y coautores y publicado en la revista “Parasites and Vectors” en el año 2020.
Figura 6. Mapa de seroprevalencia de leishmaniosis canina obtenido de Gálvez et al. Parasites Vectors (2020) 13:204: (https://parasitesandvectors.biomedcentral.com/articles/10.1186/s13071-020-04081-7.)
2.3
Haz clic en la imagen para obtener una vista más ampliada
Motivos de la expansión de la enfermedad
Diferentes factores pueden explicar la expansión de la enfermedad o la detección de casos en zonas consideradas previamente como no endémicas, como:
- El viaje de las mascotas con los tutores (factor importante considerando nuestro país como destino turístico por excelencia).
- El cambio climático ha favorecido también la expansión del vector con más zonas que mantienen actualmente un clima mediterráneo donde el vector puede sobrevivir y mantenerse como vector de la enfermedad. La época de actividad del mosquito se ha alargado y se detectan en zonas más al Norte (de España y de Europa) y a mayores altitudes.
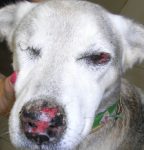
- Las otras formas posibles de transmisión, no vectoriales, en áreas donde los vectores estén ausentes, aunque dichos modos de transmisión probablemente solo tengan un papel marginal en la epidemiología de las infecciones en el perro.
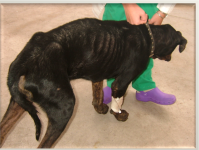
Figura 7. Perro con leishmaniosis.
2.4
Haz clic en la imagen para obtener una vista más ampliada
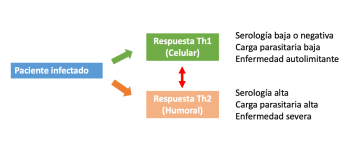
Respuesta inmunitaria en el hospedador
En muchas ocasiones se cita que la leishmaniosis es una enfermedad “inmunomediada” más que una enfermedad infecciosa, porque la interacción del parásito con el sistema inmunitario y la respuesta de este es la que va a determinar la gravedad de la enfermedad en un hospedador. Clásicamente se caracterizan a los pacientes como aquellos con una respuesta inmunitaria principalmente de tipo celular (Th1) que son aquellos que van a controlar mejor la enfermedad, o con una respuesta predominantemente humoral (Th2) en los cuales la enfermedad es más severa. El balance entre la respuesta humoral y celular en el paciente es lo que va a determinar el amplio espectro posible de enfermedad y las manifestaciones clínicas.
Figura 8.

Módulo: Leishmaniosis canina y felina – ¿entendemos cómo funciona la enfermedad?
Parte 3


3.1
Haz clic en la imagen para obtener una vista más ampliada
¿Por qué hay perros más susceptibles a la leishmaniosis?
El sistema inmunitario y la base genética son claves en la susceptibilidad a la enfermedad. Razas como Bóxer, Pastor Alemán, Rottweiler y Cocker Spaniel son más susceptibles, mientras que otras como el Podenco Ibicenco parecen más resistentes. También influyen la edad, el estado nutricional, coinfecciones, carga parasitaria y cualquier factor que cause inmunosupresión.
La enfermedad muestra un patrón bimodal: es más frecuente en perros de 2-3 años y mayores de 8. Los perros jóvenes suelen presentar signos menos severos y menos alteraciones hematológicas que los adultos o geriátricos1.
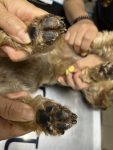
Figura 9. Perro con leishmaniosis.
1 Cabré M. et al. Is signalment associated with clinicopathological findings in dogs with leishmaniosis? Vet Rec 2021; e451.
3.2
Haz clic en la imagen para obtener una vista más ampliada
¿Cuáles son los mecanismos de patogenicidad?
Los signos clínicos de la leishmaniosis se producen principalmente por dos mecanismos patogénicos:
- Lesión directa por presencia del parásito en los lugares donde se multiplica, causando inflamación en dichos tejidos, que puede tener un carácter macrofágico, neutrofílico o lifoplasmocítico.
- Depósito de inmunocomplejos en distintas zonas anatómicas, por fenómenos de hipersensibilidad tipo II o III, que al depositarse en los tejidos provocan activación de fagocitos y daño tisular, con lesiones principalmente renales, oculares, articulares y vasculares. También pueden desarrollarse autoanticuerpos en algunos casos.
Figura 10.
3.3
Haz clic en la imagen para obtener una vista más ampliada
Signos clínicos de leishmaniosis
Los signos más clásicos y frecuentes son las alteraciones dermatológicas (dermatitis exfoliativa, onicogrifosis, lesiones ulcerativas, dermatitis papular, hiperqueratosis, etc.), presentes en el 80 % de los perros enfermos, junto con manifestaciones inespecíficas como pérdida de peso, linfadenomegalia, apatía, atrofia muscular, hepatomegalia y/o esplenomegalia. La prevalencia de enfermedad renal varía entre un 16-52 %, según estudios. Es frecuente la proteinuria, pero no tanto la azotemia o enfermedad renal avanzada. La lesión renal más común se debe al depósito de inmunocomplejos en el glomérulo, causando glomerulonefritis e inflamación intersticial. Otros signos clínicos, de frecuencia variable, incluyen alteraciones oculares, digestivas, articulares, neurológicas, musculares y cardíacas.
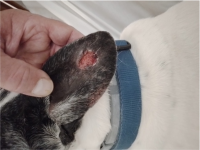
Figura 11. Úlcera cutánea en un perro con leishmaniosis.
3.4
Haz clic en la imagen para obtener una vista más ampliada
Alteraciones analíticas
En un perro con leishmaniosis se debería de revisar el hemograma, bioquímica sérica, proteinograma y análisis de orina. Hay alteraciones que son sugestivas, pero no patognomónicas de la enfermedad, por lo que hay que considerar siempre otros diagnósticos diferenciales.
Hay algunas alteraciones laboratoriales más frecuentes como la anemia no regenerativa normocítica normocrómica, leucograma de estrés, trombocitopenia (menos común), alteraciones de las proteínas plasmáticas (hiperglobulinemia, más frecuente por gammapatía policlonal; hipoalbuminemia, compensatoria o por nefropatía perdedora de proteínas), proteinuria, azotemia y/o leve incremento de enzimas hepáticas.
Figura 12. Alteraciones analíticas compatibles con leishmaniosis (Adaptado de Paltrinieri S et al. Vet Clin Pathol 45/4 (2016) 552-578).

Módulo: Leishmaniosis canina y felina – ¿entendemos cómo funciona la enfermedad?
Parte 4


4.1
Haz clic en la imagen para obtener una vista más ampliada
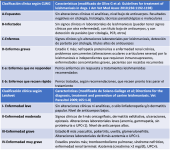
Clasificación de perros con leishmaniosis
En zonas endémicas hay perros sanos no infectados, infectados sanos, infectados enfermos, o enfermos por otro proceso. Por eso, es clave interpretar en conjunto la historia clínica, el examen físico, las alteraciones laboratoriales y las pruebas diagnósticas para clasificar al paciente en estadios clínicos. Esto orienta el manejo, la necesidad de tratamiento leishmanicida y otras terapias de soporte.
Las clasificaciones más usadas son las de LeishVet y el “Canine Leishmaniosis Working Group (CLWG)”, que han desarrollado guías con protocolos y recomendaciones adaptados a cada fase de la enfermedad.
Figura 13. Clasificación clínica de perros con leishmaniosis.
4.2
Haz clic en la imagen para obtener una vista más ampliada
Diagnóstico de leishmaniosis
El diagnóstico debe basarse en un juicio clínico que combine la historia, el examen físico, las alteraciones laboratoriales y las pruebas específicas. Lo ideal es emplear métodos que valoren la respuesta inmune (serologías) y la detección directa del parásito (citologías, PCR, IHC, etc.).
Las serologías detectan anticuerpos frente a L. infantum (IgG). Las pruebas rápidas cualitativas son menos sensibles que las cuantitativas. La titulación de anticuerpos ayuda a clasificar la infección. Al monitorizar, es clave usar siempre la misma técnica cuantitativa, ya que hay diferencias en sensibilidad y especificidad entre métodos.
Figura 14. Guías de diagnóstico y manejo de la leishmaniosis en perros.
4.3
Haz clic en la imagen para obtener una vista más ampliada
Pruebas de detección directa del parásito
Citologías de médula ósea, linfonodos o lesiones compatibles permiten detectar amastigotes intracelulares en macrófagos o libres. Las técnicas moleculares pueden identificar el parásito en sangre, médula ósea, hisopos conjuntivales, etc., y cuantificar la carga parasitaria mediante qPCR. Esta última puede tener valor pronóstico: cargas medias-altas se asocian a mayor riesgo de enfermedad, incluso con títulos bajos de anticuerpos. No obstante, la PCR debe interpretarse con cautela en zonas endémicas, ya que puede haber positivos en perros asintomáticos. También pueden realizarse pruebas moleculares o tinciones inmunohistoquímicas sobre muestras de biopsias de piel u otras localizaciones.
Figura 15. Macrófago con amastigotes de Leishmania spp. en citología de médula ósea.
4.4
Haz clic en la imagen para obtener una vista más ampliada
Tratamiento de perros con leishmaniosis
El tratamiento depende del estadio clínico. Se usan leishmanicidas en perros infectados con signos clínicos, siguiendo guías de expertos. La opción más común es alopurinol con antimoniales. También puede combinarse alopurinol con miltefosina, aunque su efecto es más lento y podría haber más recaídas.2 Si aparece xantinuria, puede ajustarse la dosis, usar dieta y/o sustituir alopurinol por nucleótidos (Impromune®).
Además del tratamiento antiparasitario, se requiere soporte según los signos clínicos, uso de repelentes para evitar reinfecciones y posibles contagios, e inmunomoduladores como domperidona o nucleótidos. También es esencial valorar y tratar enfermedades concomitantes, sobre todo en perros geriátricos.
Figura 16. Tabla de protocolos recomendados de tratamiento de leishmaniosis en el perro.
2 Manna L et al. Parasites and Vectors 2015; 8;289.

Módulo: Leishmaniosis canina y felina – ¿entendemos cómo funciona la enfermedad?
Parte 5


5.1
Haz clic en la imagen para obtener una vista más ampliada
Seguimiento
El seguimiento varía según el estadio clínico. En seropositivos sanos debe hacerse una monitorización estrecha para detectar progresión, aunque muchos mantienen títulos bajos o seronegativizan. En perros en tratamiento, se aconseja control a los 3-5 días por posible empeoramiento inicial (formación de inmunocomplejos). Se han descrito casos de pancreatitis con antimoniales, por lo que debe valorarse si hay signos compatibles. La función renal debe reevaluarse al mes, valorando proteinuria y necesidad de tratamiento antiproteinúrico. Según las alteraciones iniciales, los controles incluirán hemograma, bioquímica, proteinograma, orina, serologías o qPCR. Los inmunocomplejos circulantes podrían ser útiles, aunque aún no están disponibles.
Figura 17. Recomendaciones de monitorización de un perro con leishmaniosis.
5.2
Haz clic en la imagen para obtener una vista más ampliada
¿Son frecuentes las recaídas?
Es clave mantener una buena salud general y controlar enfermedades concomitantes para evitar recaídas. Incluso sin inmunosupresión, hasta un 20 % de los perros pueden recaer, normalmente en el primer año tras el tratamiento, con signos similares a los iniciales.3 Las causas pueden ser mal cumplimiento, reinfección, reactivación o, menos frecuentemente, resistencia (que suele aparecer durante o poco después del tratamiento). El alopurinol de por vida no previene reinfecciones y no se recomienda su uso indefinido, por riesgo de efectos secundarios como xantinuria o urolitiasis.
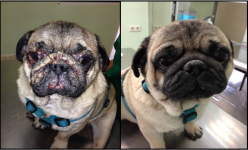
Figura 18. Lesiones cutáneas en un perro antes y después del tratamiento leishmanicida.
3 Lluis Ferrer. The conundrum of clinical relapses in canine leishmaniosis. Proceedings of ALIVE 2 Congress, Nice, 18-24 April 2024.
5.3
Haz clic en la imagen para obtener una vista más ampliada
Leishmaniosis en gatos I
La leishmaniosis felina se diagnostica con más frecuencia y puede presentarse con cuadros clínicos variados. Muchos gatos afectados tienen comorbilidades, como infección por FIV.
Las revisiones de casos muestran que las lesiones cutáneas (dermatitis exfoliativa, ulcerativa o nodular) aparecen en casi el 70 % de los casos, pero también se observan signos oculares (uveítis, conjuntivitis), renales, inespecíficos (linfadenomegalia, mal estado general), rinitis o enteropatía. La hiperproteinemia es la alteración más común en analítica.
En general, si en un perro con un cuadro clínico determinado sospecharíamos de leishmaniosis, en un gato con la misma presentación deberíamos de incluir la leishmaniosis también en el diagnóstico diferencial.
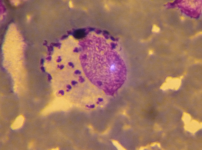
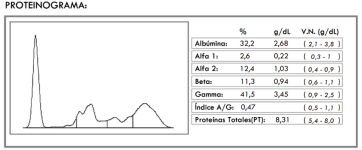
Figura 19. Gammapatía policlonal en un gato con leishmaniosis.
5.4
Haz clic en la imagen para obtener una vista más ampliada
Leishmaniosis en gatos II
El diagnóstico en gatos puede ser más complejo, pero lo primero es sospecharla e incluirla en el diagnóstico diferencial si el cuadro clínico es compatible.
Se confirma combinando la sospecha clínica (signos y alteraciones analíticas) con serologías y pruebas de detección directa del parásito. Los títulos de anticuerpos suelen ser más bajos y variables que en perros, por lo que es útil combinarlos con citologías, PCR u otras técnicas que confirmen la presencia del parásito.
No existe un tratamiento estandarizado. El fármaco más usado es alopurinol, a veces combinado con antimoniales en casos seleccionados.
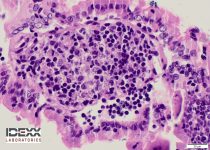
Figura 20. Biopsia intestinal de un gato con enteropatía por leishmaniosis (anatomía patológica realizada en Laboratorios IDEXX).
Sigue formándote en "Cómo afecta la leishmaniosis a la piel y cómo no volverse loco en el diagnóstico" de la mano de Seresto® y Advantix® de Elanco



WhatsVet | Leishmaniosis cutánea – su compleja fisiopatología da lugar a cuadros clínicos muy diversos
Autoría: Annabel Dalmau, LV, Acred Derm AVEPA, Full Member ESVD, Comité científico GEDA, AniCura Mediterrani Hospital Veterinari.
Podcast | 10 audiotips: La leishmaniosis cutánea: una enfermedad con tantas caras que debemos incluirla en muchos diferenciales
Autoría: Annabel Dalmau, LV, Acred Derm AVEPA, Full Member ESVD, Comité científico GEDA, AniCura Mediterrani Hospital Veterinari.
WhatsVet | ¿Cómo elegir el mejor método diagnóstico en cada caso de leishmaniosis cutánea?
Autoría: Annabel Dalmau, LV, Acred Derm AVEPA, Full Member ESVD, Comité científico GEDA, AniCura Mediterrani Hospital Veterinari.
Podcast | 11 audiotips: La importancia de la prevención y opciones de tratamiento
Autoría: Annabel Dalmau, LV, Acred Derm AVEPA, Full Member ESVD, Comité científico GEDA, AniCura Mediterrani Hospital Veterinari.
EM-ES-25-0066